Por María Luisa Santillán. Ciencia UNAM-DGDC
Cuando miramos hacia el cielo, si está despejado podemos ver el color azul que lo caracteriza, algunas nubes e incluso veremos pasar aviones o aves. Son cosas visibles ante nuestros ojos. También, aunque no las notamos, en esos espacios, y mucho más arriba de ellos, ocurren cientos de reacciones químicas que permiten que la vida se lleve a cabo tal y como la conocemos.
Así, en las distintas capas que componen la atmósfera (esa delgadísima capa gaseosa que rodea al planeta) se pueden encontrar gases y partículas sólidas y líquidas que tienen distintas funciones, por ejemplo, permiten una regulación de la temperatura, nos protegen de la radiación ultravioleta y son un elemento fundamental para la vida en el planeta.
Identificar y medir esos gases ha sido una labor de muchos años y en la que han participado científicos de todo el mundo. Por ejemplo, en el caso del ozono hay quien dice que ya Homero, en su libro La Odisea, hablaba de él sin nombrarlo aún como ozono. Tuvo que ser hasta 1840, cuando el alemán Christian Friedrich Schönbein lo descubriera, ya que lo identificó por su fuerte olor, aisló el compuesto gaseoso y lo denominó ozono, que proviene de la palabra griega ozein, que significa oler.
Unos años después, en 1865, Jacques-Louis Soret, logró descubrir su composición química, que es O3. En 1913, los franceses Charles Fabry y Henri Buisson descubrieron la capa de ozono. Y para 1920, el meteorólogo británico G. Dobson construyó un espectrómetro que le permite medir el ozono atmosférico.
Además de identificarlo y poderlo medir, también las investigaciones se han enfocado en conocer qué daña nuestra capa de ozono y cómo es que las moléculas de este elemento pueden destruirse.
Por seguir estos procesos, el investigador mexicano Mario Molina, junto con el estadounidense Frank Sherwood Rowland y el holandés Paul Crutzen, recibieron el Premio Nobel de Química en 1985 “por sus investigaciones sobre la química atmosférica y la predicción del adelgazamiento de la capa de ozono como consecuencia de la emisión de ciertos gases industriales, los clorofluorocarburos (CFCs), publicadas en un artículo en la revista Nature en junio de 1974”.
¿Qué la afecta?
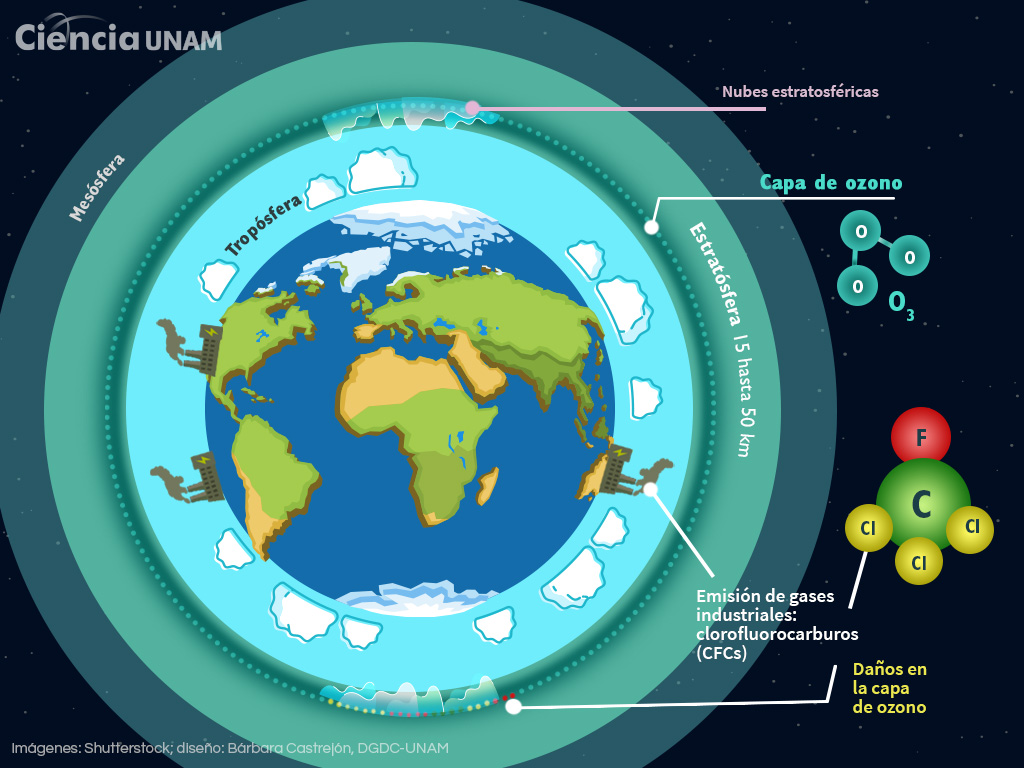
La capa de ozono se localiza a unos 15 hasta 50 km de la superficie de la Tierra–en la región conocida como estratósfera–. Nos protege de la radiación ultravioleta, pues estar expuestos a altos niveles de ésta puede causar enfermedades, dañar a los animales, las plantas y los microbios. Y aunque esta capa es fundamental para la vida, también es frágil y ha sufrido demasiados embates por parte de los humanos.
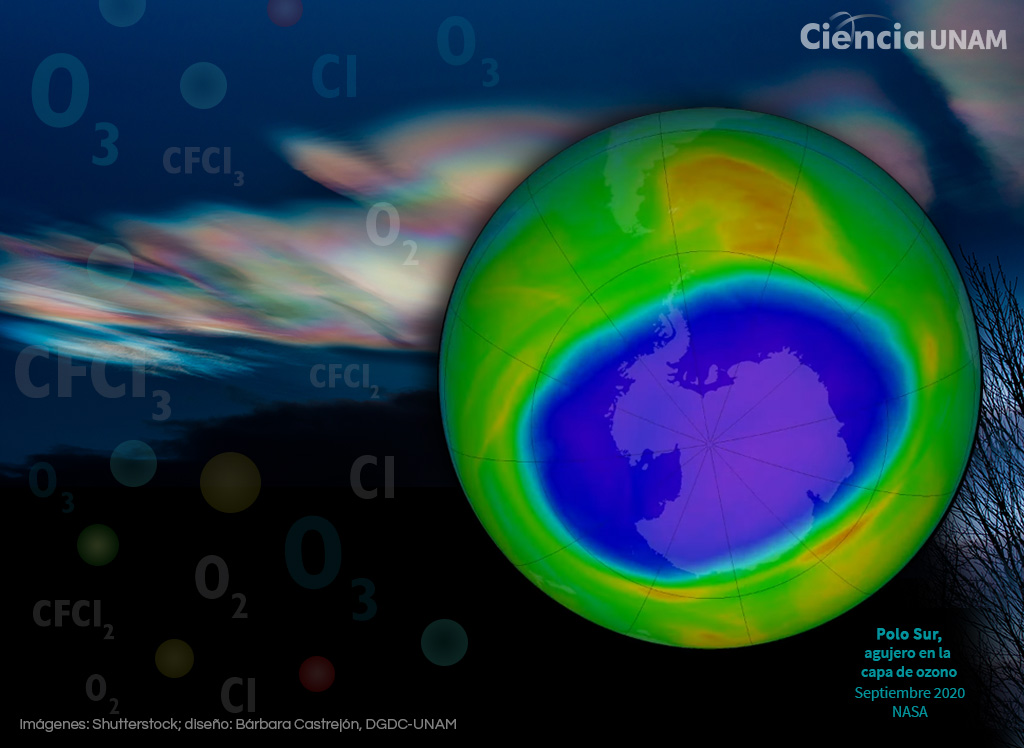
Uno de ellos fue cuando se descubrió que había un agujero en esta capa, el cual tenía como una de sus fuentes de destrucción a los CFCs, gases que se descomponían al llegar a la estratósfera, liberando átomos de cloro que destruirían al ozono. Estos CFC se encuentran en los refrigerantes, los aerosoles, el aire acondicionado y como agentes espumantes para la fabricación de espumas plásticas.
Frente a esta situación, en 1987, se estableció el Protocolo de Montreal, un acuerdo internacional que buscó proteger la capa de ozono, entre otras cosas, disminuyendo la emisión de CFC a la atmósfera. Fue adoptado enseguida por varios países y de acuerdo con la doctora Graciela Binimelis de Raga, del Centro de Ciencias de la Atmósfera de la UNAM, su ratificación por casi todos los países del mundo “es un ejemplo de éxito de lo que se puede lograr si todos los países deciden que sí van a hacer algo al respecto”.
La investigadora, responsable del grupo de Interacción Micro y Mesoescala, destaca que una vez que se prohibieron los CFC se empezaron a utilizar los hidrofluorocarbonos (HFC), los cuales ya no destruían la capa de ozono, pero sí ocasionaban otros problemas porque son gases de efecto invernadero.
“El problema que hay con estos gases es que cada molécula de éstos tiene 1600 veces más potencial de calentamiento que el bióxido de carbono, por lo que nada más los HFC contribuirían a un aumento de temperatura global entre 0.3 y 0.5 grados al fin del siglo. La Enmienda de Kigali al Protocolo de Montreal ahora prohíbe su uso y en lugar de tener este calentamiento sólo tendríamos como 0.05 de grado a fin del siglo, una diferencia muy importante.”
Agujero y dinámica atmosférica
El problema del hoyo de ozono no es sólo químico, es de la dinámica de la atmósfera, destaca la especialista en física de partículas atmosféricas y nubes. Por lo tanto, no importa en dónde emitamos contaminantes, la atmósfera no tiene fronteras y eventualmente llegarán a todos lados.
Esto pudo comprobarse cuando el agujero de la capa de ozono apareció en la Antártida, un sitio poco habitado y con ninguna fuente de emisión de contaminantes, en comparación de los que se emiten a la atmósfera en las grandes ciudades.
¿Por qué se originó el agujero en esta zona? Lo que se requiere en la práctica para que se destruyan las moléculas de ozono es que se formen nubes estratosféricas polares, que son cristales. Dichas nubes se generan a temperaturas muy bajas, entre 60 u 80 grados bajo 0, las cuales sólo se encuentran en las regiones polares cuando es de noche.
En estas condiciones, los vientos polares, que circulan alrededor del polo, son muy fuertes, impiden que el aire se mezcle y permiten que la masa de aire continúe enfriándose durante los meses que no recibe nada de radiación solar. Una vez que está muy fría, se generan estas nubes estratosféricas necesarias para que se lleve a cabo la reacción que destruye el ozono.
De esta manera, en septiembre, cuando empieza a llegar la radiación solar en el Hemisferio Sur, interactúa con las moléculas gaseosas y con los cristales que forman las nubes estratosféricas y se produce la reacción química que destruye las moléculas de ozono. En primavera y verano, la intensidad del vórtice polar disminuye y permite una mezcla de aire polar en la estratosfera con aire proveniente de zonas subtropicales con mayor concentración de ozono que llega hasta la zona polar y en esencia se llena el agujero, explica la investigadora.
El Hemisferio Norte también tiene vórtice polar, aunque los vientos son más intensos en el Hemisferio Sur. Además, en el norte se perturban porque hay más masa continental, y a pesar de que también ocurren ahí los procesos químicos que destruyen al ozono, hay mayor mezcla de masas de aire que proceden de la zona ecuatorial y se desplazan hacia la estratosfera polar, llevando ozono que se forma más en estas zonas tropicales.
Recuperación de la capa de ozono
Gracias al conocimiento que se tiene sobre la capa de ozono, la producción y destrucción del ozono, el surgimiento del agujero y qué lo provoca, es que se pudieron realizar distintas acciones a nivel mundial que han permitido que en la actualidad el uso de CFCs y otros compuestos esté prohibido, lo cual ha ayudado a que haya una recuperación del agujero de la capa de ozono.
Asimismo, se sigue monitoreando su emisión, a través de satélites o instrumentos como el espectrómetro de Dobson que permiten detectar distintas moléculas por espectroscopia. Porque, destaca la doctora Raga, entre las cosas que se saben es que en 1950 aún no había muchas de las sustancias que hoy se encuentran en la capa de ozono, las cuales empezaron a producir daños a partir de su elaboración industrial y emisiones a la atmósfera. Dicha situación puso en alerta a los científicos en el mundo y se logró la reducción de estos gases con la llegada del Protocolo de Montreal.
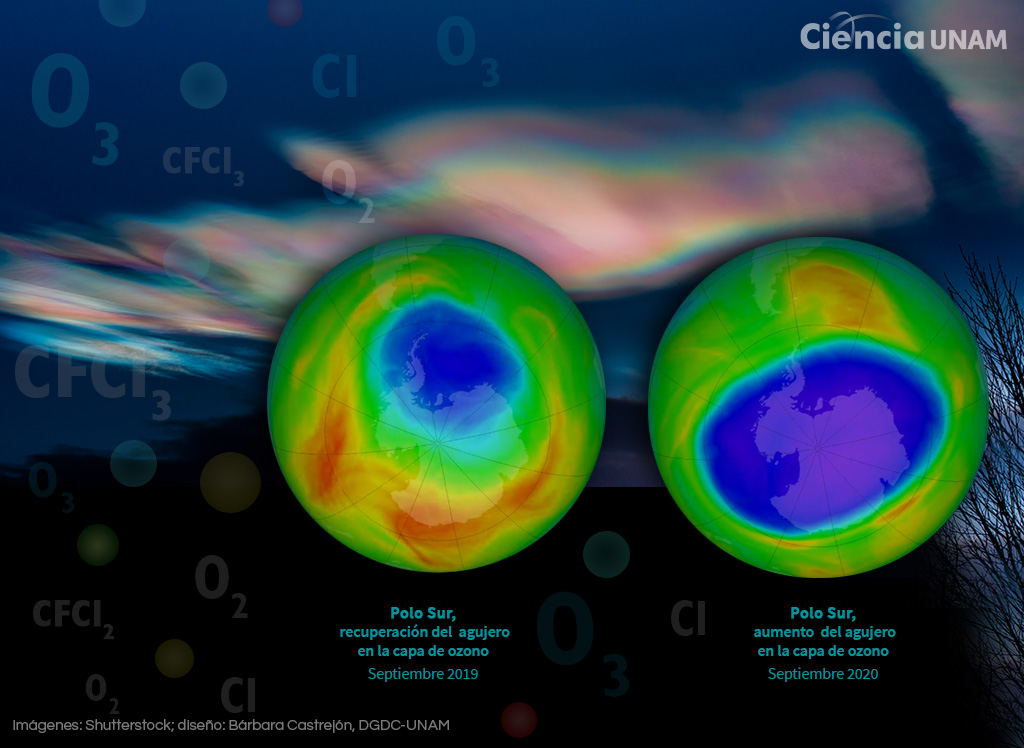
“Todavía se produce la destrucción, porque no es que haya cero concentración de todas estas emisiones, pero ya no se observan esos hoyos tan enormes como se vieron en los primeros años, ya se ha ido recuperando. La concentración de ozono entre 2008 y 2012 todavía fue de 2.5% menos que la que había entre 1964 y 1980, pero ya no 5% menos; se ha recuperado ya como la mitad y para el 2050 se espera que esté completamente recuperada”, concluye la doctora Raga.
Consulta la nota original: https://ciencia.unam.mx/leer/1110/la-capa-de-ozono-elemento-fundamental-en-la-dinamica-atmosferica
- Más allá de la apatía: juventudes y compromiso ambiental - marzo 19, 2026
- Plumas NCC | Nuevo paradigma del gobierno corporativo en México frente a la disrupción tecnológica - marzo 17, 2026
- NCC Radio – Emisión 354 – 16/03/2026 al 22/03/2026 –El murciélago perdido de Antioquia reaparece tras 24 años - marzo 16, 2026