EE.UU.
Vacunar a más personas con mayor rapidez: la empresa estadounidense Johnson&Johnson ha solicitado la aprobación de emergencia en EE.UU., a la que seguirá en breve una solicitud para la UE.
Es una muy buena noticia que la empresa estadounidense Johnson & Johnson (J&J) haya solicitado ahora también a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) la aprobación de emergencia de su vacuna contra el COVID-19. En las próximas semanas se presentará también una solicitud de aprobación de emergencia ante la autoridad de medicamentos de la Unión Europea, la EMA.
Los datos evaluados del ensayo de fase III sugieren que la vacuna de J&J reduce el riesgo de una enfermedad de COVID-19 moderada o grave en un 66 por ciento cuatro semanas después de la vacunación.
El hecho de que esta cifra sea inferior a la de las vacunas aprobadas con anterioridad probablemente tenga que ver con las nuevas mutaciones que aún no habían aparecido durante sus ensayos a finales del verano pasado.
Ventajas evidentes
Pero la vacuna de J&J también tiene algunas ventajas claras: solo es necesario inyectarla una vez, lo que significa que un mayor número de personas podría recibir la protección de la vacuna mucho más rápidamente. No obstante, las pruebas posteriores deberían aclarar si la eficacia podría aumentar aún más con dos dosis de vacunación, como es el caso de los competidores.
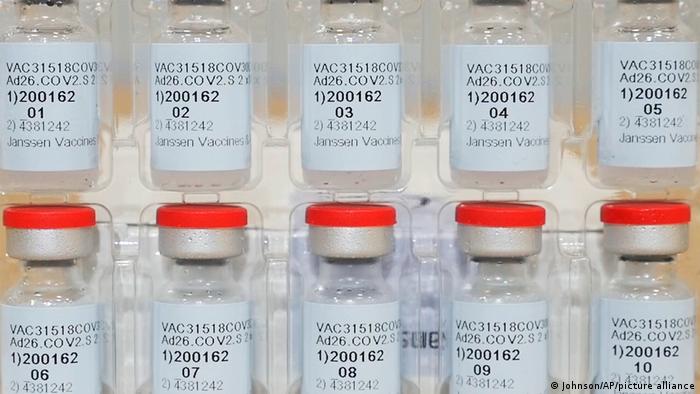
La vacuna de J&J puede transportarse y almacenarse a temperatura de frigorífico
Además, la vacuna de J&J puede transportarse y almacenarse a temperatura de frigorífico porque, a diferencia de las vacunas de BioNTech/Pfizer y Moderna, es una vacuna vectorial basada en un virus del resfriado normal. En términos de diseño, la vacuna de J&J es similar a la de AstraZeneca. Ambos se centran en la proteína espiga de la superficie del virus que desencadena la respuesta inmunitaria protectora.
Afortunadamente, el ensayo de fase III, en el que participaron 44.000 personas en EE.UU., Brasil y Sudáfrica, demostró que la vacuna funciona tan bien en personas mayores como en jóvenes, algo que se había puesto en duda con la vacuna de AstraZeneca. Un tercio de los participantes en el ensayo de la vacuna de J&J eran mayores de 60 años. Lo más importante es que ninguno de los vacunados por J&J murió o fue hospitalizado, lo cual es un signo alentador.
Hasta 400 millones de dosis de vacunas para la UE
Tan pronto como la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) dé el visto bueno, podrán comenzar las entregas, anunció Johnson & Johnson. La empresa tiene previsto suministrar un total de mil millones de dosis este año. La producción se llevará a cabo en Estados Unidos, Europa, Sudáfrica e India.
Estados Unidos ha conseguido 100 millones de dosis por 1.000 millones de dólares, que J&J tiene previsto enviar en el primer semestre del año. Además, Estados Unidos tiene una opción para otros 200 millones de dosis. La UE se ha asegurado hasta 400 millones de dosis de la vacuna.
Por: Deutsche Welle (DW).
- Plumas NCC | Rendición cognitiva y la pérdida de la autoría de las ideas - mayo 25, 2026
- NCC Radio – Emisión 364 – 25/05/2026 al 31/05/2026 – Con cultivo de ajolotes en México buscan cura de enfermedades - mayo 25, 2026
- Islas de plástico se convierten en hábitat de especies marinas - mayo 25, 2026







