México.
Cuando nos sentimos enfermos podemos curarnos al ingerir una tableta o cápsula, colocarnos una inyección o untarnos una pomada que nos puede aminorar o eliminar aquel padecimiento que nos aqueja. Detrás de ese alivio que sentimos hay miles de años de conocimiento previo sobre qué planta o compuesto químico nos brinda una mejoría ante algún malestar físico, los cuales nosotros vemos reflejados en un fármaco.
Los fármacos son moléculas que al ingresar a nuestro cuerpo se dirigen a un blanco molecular (que generalmente son proteínas) y se unen a él con el fin de generar un efecto terapéutico.
“En la actualidad, hay mucha información de compuestos que tienen actividad sobre diferentes blancos terapéuticos (enzimas, transportadores, receptores), ya sabemos más o menos cómo funciona y tenemos programas de modelado molecular donde podemos observar estas interacciones”, explica el doctor Rodrigo Aguayo Ortiz, de la Facultad de Química de la UNAM.
Sin embargo, sintetizar compuestos y hacerles modificaciones para crear un fármaco es costoso, difícil de realizar, es un proceso largo y requiere de mucho personal.
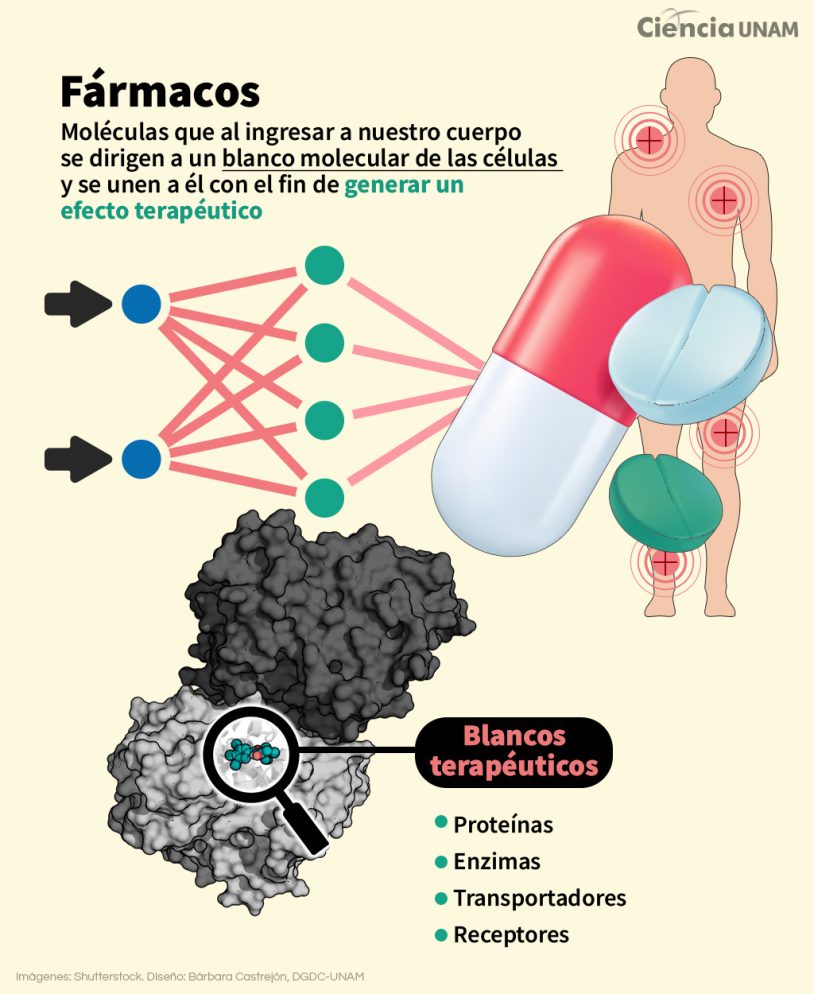
Imagen vía Ciencia UNAM
Actualmente diversas empresas farmacéuticas tienen una molécula y empiezan a modificar su estructura tratando de mejorar su actividad, sin embargo, hacer esto no siempre lleva a encontrar el resultado deseado. La propuesta del grupo de investigación del doctor Aguayo Ortiz consiste en generar fármacos diseñados por computadora, a través del uso de herramientas computacionales de modelado molecular para estudiar las interacciones –a nivel atómico– del ligando con su proteína.
Estas interacciones son fundamentales porque permiten entender por qué un fármaco actúa de una manera en la proteína, qué cambios se dan en ella, qué reacción tendría un organismo al tomar un fármaco, si va a generar una mejor actividad o va a presentar un efecto secundario.
Entonces, el diseño de fármacos por computadora, según el doctor Aguayo, permitiría que en lugar de hacer muchas modificaciones a una sustancia hasta encontrar su mejor actividad, sólo evalúan el perfil de interacción que tiene el fármaco con la proteína, y proponen algunas modificaciones con base en él.
Esto representa un costo mucho menor que trabajar un fármaco de la forma tradicional, además de que les permitiría proponer menos compuestos y que éstos tengan una mejor actividad en el organismo.
“El diseño de fármacos asistido por computadoras consiste en basarnos en toda la información experimental y de actividad biológica que tenemos en bases de datos y con métodos computacionales reducir esa información, tratar de condensar todo lo que nos están dando los datos experimentales y llegar a una conclusión rápida de modificación. La idea es simplificar mucho más la vía de obtención de un fármaco”.
Además de estudiar la interacción proteína-ligando para diseñar fármacos, también se utilizan otras herramientas computacionales para predecir y tratar de identificar características de estos compuestos que puedan dar toxicidad o aumentar el metabolismo del fármaco.
“Con métodos computacionales podemos proponer modificaciones estructurales para ver si va a funcionar igual el fármaco, pero eso basado en la interacción proteína-ligando, ver que no vamos a afectar la interacción del fármaco con la proteína y que al quitar un grupo funcional o una región no genere toxicidad en la persona”.
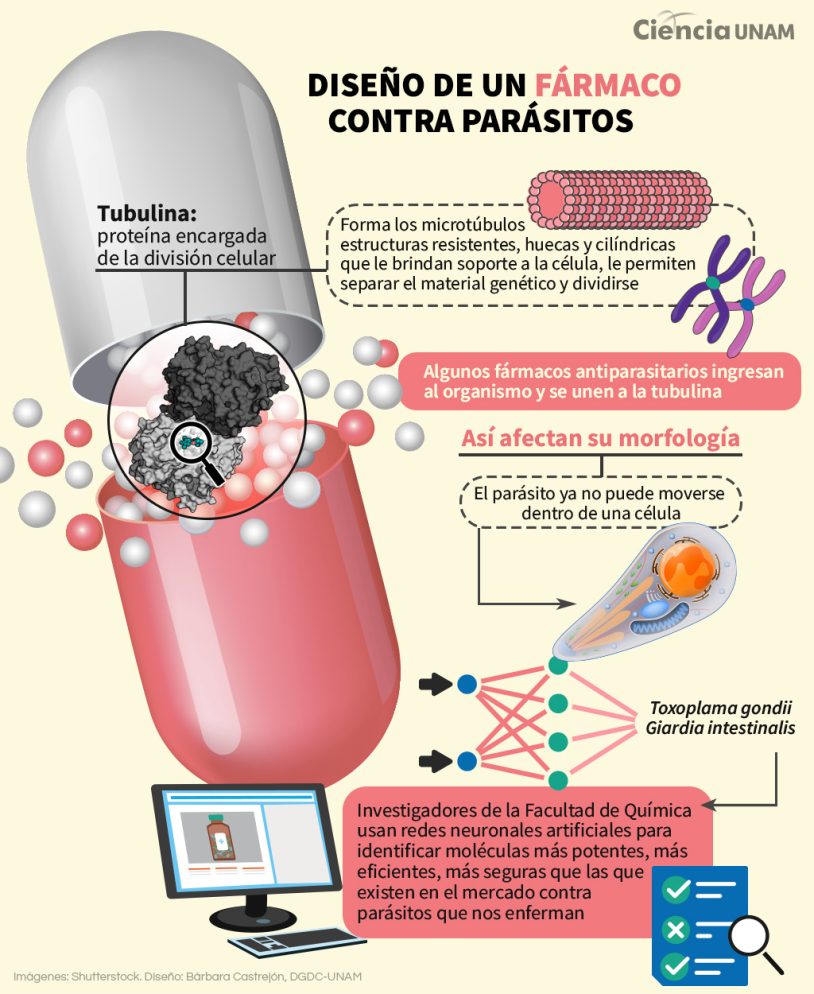
Imagen vía Ciencia UNAM
Alternativas contra parásitos
El grupo de trabajo del doctor Rodrigo Aguayo se ha enfocado en el diseño de fármacos con actividad antiparasitaria y anticancerígena.
Los parásitos tiene varias similitudes con las células del humano, una de ellas es que ambos tienen una proteína conocida como tubulina y que es un blanco terapéutico sobre la cual un fármaco puede actuar para tener un efecto terapéutico.
La tubulina es la encargada de la división celular; forma los microtúbulos, que son unas estructuras resistentes, huecas y cilíndricas que le brindan soporte a la célula, le permiten separar el material genético y que las células se dividan.
Existen fármacos antiparasitarios que cuando ingresan al organismo se pegan a la tubulina, lo cual tiene efectos en su morfología, es decir, el parásito experimenta cambios, ya no puede viajar, moverse dentro de una célula y no se puede dividir.
Hace algunos años encontraron que fármacos antiparasitarios como el mebendazol y el albendazol, actuaban contra ciertos parásitos, pero no se sabía en dónde se unían con la tubulina para generar un efecto terapéutico.
“Si no sabes dónde ¿cómo propones nuevos fármacos, cómo puedes mejorar la estructura? Lo que nosotros hicimos fue, con base en toda la información experimental, proponer el posible sitio de unión de estos compuestos en la tubulina, encontramos el sitio y empezamos a proponer modificaciones de los compuestos. Tiempo después experimentalmente se demostró que sí era el sitio que habíamos propuesto”.
Asimismo, han notado que el mecanismo de acción de la tubulina es similar en células cancerosas, por ello el grupo de investigación que dirige el doctor Aguayo también estudian esta proteína en compuestos anticancerosos, con el fin de evitar que se dividan las células cancerosas.
El investigador destaca que este es un ejemplo de cómo los métodos computacionales funcionan si se basan y apoyan en datos experimentales. “Nos hemos dado cuenta que este blanco terapéutico que nosotros seleccionamos [la tubulina] nos permite atacar a estos dos padecimientos, tanto parásitos como cáncer”.
En cuanto a parásitos trabajan con Toxoplama gondii y Giardia intestinalis, en tanto los estudios que realizan en cáncer son en leucemia y cáncer de pulmón. “Ahorita ya encontramos que los métodos nos han ayudado a obtener moléculas activas. El siguiente paso es encontrar moléculas que sean más potentes, más eficientes, más seguras que las que ya existen en el mercado”.
Combinar métodos
En la actualidad, no existe un fármaco que haya sido creado exclusivamente por computadora, “porque siempre vamos a necesitar un respaldo experimental”, explica el investigador. Sin embargo, sí hay un fármaco antiviral dirigido al VIH para el cual se llevó un proceso de optimización con métodos computacionales, con el fin de ver cómo interactuaba con la proteasa (una enzima que descompone las proteínas) del virus del VIH. Y gracias a esta información pudieron llegar a ese compuesto.”
“El método computacional es una parte del proceso de optimización para llegar al fármaco”, afirma.
El diseño de fármacos por computadora surgió casi al mismo tiempo que cuando se empezaron a usar las computadoras. Un antecedente es el caso de las Relaciones Cuantitativas Estructura-Actividad (QSAR, por sus siglas en inglés), que es una metodología computacional que consiste en usar métodos cuantitativos y modelos matemáticos que permitieron predecir la actividad de una molécula.
Actualmente también se utilizan redes neuronales artificiales para compilar la amplia cantidad de datos y generar modelos moleculares más robustos. “De tal forma que nosotros le damos una molécula y si la red neuronal está hecha para predecir toxicidad, esa red neuronal, con todo lo que tiene de conocimiento, nos va a decir con más precisión si es tóxica o no”.
Al inicio de los 2000 creció el interés por conocer las interacciones proteína-ligando, porque la base de datos de Protein Data Bank (PDB), que recopila la estructura tridimensional de las proteínas, empezó a compilar más información sobre éstas, la cual está disponible para quien quiera hacer investigación.
Sin embargo, el mayor avance ocurrió en 2020 con el surgimiento del AlphaFold, un programa de Inteligencia rtificial que predice la estructura de las proteínas. Incluso en 2024 los creadores de esta herramienta recibieron el Premio Nobel de Química.
Finalmente, el doctor Aguayo Ortiz destaca que uno de los problemas que existen hoy en día es el exceso de información disponible en estas bases de datos, por lo que recomienda ser muy cuidadosos con su uso, hacer un análisis y una adecuada curaduría de los datos.
- Lluvia ácida: contaminación que regresa con graves impactos - marzo 2, 2026
- Súper electrodos mejoran prótesis y comunicación muscular - marzo 2, 2026
- Universidad honra legado de Gabriela Mistral con doctorado - marzo 2, 2026







