España.
Un equipo del ICM-CSIC, en colaboración con el Instituto de Investigación Biomédica de Bellvitge, ha creado dos nuevas herramientas de edición genética, ‘tijeras’ genéticas cuyas patentes están en trámite. Los sistemas tienen características únicas respecto al más utilizado, el CRISPR Cas9 procedente de la bacteria Streptococcus pyogenes.
En 2010, la expedición Malaspina circunnavegó el planeta a bordo del buque oceanográfico Hespérides para estudiar, durante casi un año, el impacto del cambio climático en el mar y explorar su biodiversidad, especialmente la de las profundidades.
Como resultado, obtuvieron una robusta base de datos genéticos microbianos que, aún hoy, esconde secuencias genéticas de interés para la biomedicina y la biotecnología. Un ejemplo son los sistemas de edición genética CRISPR Cas9 que han revolucionado la ciencia de este siglo por su capacidad de eliminar, editar o introducir nuevos genes en organismos.
Las tijeras genéticas que más se usan en los laboratorios de todo el mundo, SpCas9, se descubrieron en el microorganismo Streptococcus pyogenes, una bacteria patógena en humanos y que prefiere las temperaturas medias.
Para ampliar la caja de herramientas con sistemas de edición genética que trabajen a otras temperaturas o editen otros tipos de genes, hay que explorar ambientes distintos en busca de los microorganismos que las portan.
Así es como un equipo del Instituto de Ciencias del Mar del Consejo Superior de Investigaciones Científicas (ICM-CSIC), junto a un consorcio multidisciplinar, ha desarrollado dos nuevas herramientas, cuyas patentes ya están en trámite.
El equipo encontró estos sistemas en una base de datos genéticos propia, única y ahora pública, procedentes de las muestras del océano profundo de la expedición Malaspina. Como todo sistema de CRISPR-Cas9, cada herramienta consta de una proteína Cas9 y su ARN asociado, que guía la proteína hacia el lugar del ADN que debe editar.
Edición a bajas temperaturas
La microbióloga del grupo de Ecología de Microorganismos Marinos del ICM-CSIC Silvia G. Acinas, coordinadora del análisis genético de las muestras profundas de la expedición, ha liderado la investigación para encontrar las secuencias de estas nuevas tijeras de edición genética.
“Para ampliar la variedad de sistemas CRISPR-Cas9, es imprescindible buscar en ambientes distintos donde puedan haber desarrollado características diferenciadoras. Nuestras dos Cas9, que proceden del océano profundo, tienen propiedades biofísicas diferentes que pueden facilitar nuevas aplicaciones. Por ejemplo, una es capaz de cortar a temperaturas bajas de forma muy precisa”, explica la investigadora.
Abundan los artículos científicos que describen nuevos sistemas CRISPR-Cas9 procedentes de bases de datos metagenómicos, es decir, de enormes cantidades de información genética de las comunidades microbianas presentes en muestras ambientales, tomadas en suelos, aguas y hasta del aire.
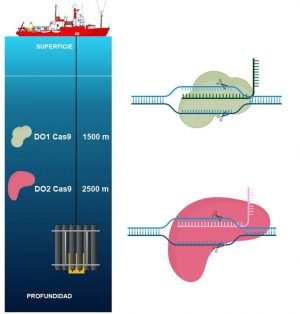
Representación del método de recogida de muestras de aguas profundas, desde el buque oceanográfico Hespérides, en las que se encontraron las dos nuevas herramientas. / Julián Cerón Madrigal
Para encontrarlos, se invierten millones en spin offs y empresas biotecnológicas como la Mammoth Biosciences de Jennifer Doudna, galardonada con el Nobel de Química en 2020 por utilizar el sistema SpCas9 en edición génica junto a Emmanuelle Charpentier.
Sin embargo, hasta ahora nadie había explorado en una base de datos del océano profundo tan completa. Además, no todos los sistemas CRISPR Cas9 que se encuentran acaban proporcionando herramientas biotecnológicas.
Alternativas al sistema CRISPR Cas9
“En el laboratorio las llamamos Astérix y Obélix porque son muy eficientes en su actividad de cortar ADN”, cuenta el investigador refiriéndose a los famosos personajes de cómic que combatían a los romanos.
“Además, funcionan bien a temperaturas más frías que el SpCas9 canónico, ampliando el rango de condiciones a las que pueden trabajar estas herramientas en los laboratorios”, revela el experto.
Por el alto potencial de transferencia de este proyecto, han recibido las ayudas CERCA GINJOL Patents Fund y BlueNetVal 2025 para que acerquen estas herramientas al mercado.
“Astérix es más pequeña que SpCas9 y, por lo tanto, más manejable en biotecnología, mientras que Obélix, más grande, tiene una secuencia de reconocimiento PAM que identifica el gen a cortar y que equivale a la de SpCas9. Gracias a esto, podemos usar nuestra Cas9 como alternativa para editar en las mismas regiones de ADN que usa SpCas9”, explica Cerón.
No obstante, en este sentido el experto subraya que “no se trata de reemplazar a SpCas9, que seguirá siendo útil, sino de ampliar la actual caja de herramientas de edición genética con nuevas variantes como las nuestras”.
Para seguir conociendo todo su potencial, ahora estudian sus índices de off target o tasa de corte fuera del gen diana, ya que las nuevas Cas9 del océano profundo parecen ser más específicas que SpCas9.
El éxito de la investigación multidisciplinar
Para Acinas, si han llegado tan lejos en el desarrollo de estas dos nuevas tijeras de edición genética es gracias al equipo multidisciplinar que hay detrás.
En el ICM-CSIC, los investigadores Pablo Sánchez y Felipe H. Countinho hicieron el análisis bioinformático de la base de datos metagenómicos que, básicamente, consiste en analizar millones de genes hasta dar con los que interesan para después evaluar su funcionamiento.
“Primero, buscamos las secuencias más parecidas a la proteína Cas9 del sistema canónico. De esa submuestra, nos quedamos con las menos parecidas a SpCas9, las más novedosas, y mandamos al laboratorio las más prometedoras para confirmar si cortaban el ADN como habíamos predicho”, explica Pablo Sánchez.
En paralelo, Francesco Colizzi, también del ICM-CSIC, estudió la estructura y dinámica de las dos Cas9 con herramientas de inteligencia artificial como la exitosa AlphaFold, reconocida con el premio nobel de Química otorgado a sus creadores en 2024, que permite hacer modelado informático 3D y estudiar la interacción entre moléculas.
“Estas proteínas poseen propiedades estructurales similares a las conocidas Cas9 a pesar de tener una secuencia bastante diferente”, cuenta el experto sobre su contribución. Sin embargo, hizo falta la colaboración externa para llegar a caracterizar los dos sistemas, es decir, comprobar experimentalmente qué secuencias cortan o su nivel de especificidad en diferentes organismos modelo.
Acinas cuenta que esto fue posible gracias a la financiación de un Proyecto de I+D+i para la realización de Pruebas de Concepto que la Agencia Estatal de Investigación le concedió en 2021, que permitió formar el consorcio de expertos DeepCas. En este sentido, la experta destaca el valor de las validaciones hechas en diversos organismos, desde plantas hasta peces, pasando por microorganismos y células humanas in vitro.
El apoyo especial de Francis Mojica
La colaboración científica tuvo un papel fundamental desde los primeros compases del proyecto, que también ha involucrado a uno de los padres de los sistemas CRISPR.
Para decidir en cuáles centrarse, de entre todos los que habían encontrado, contaron con el apoyo de Francis Mojica, la persona que en 2001 acuñó el término CRISPR por las siglas en inglés de “repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas” y uno de los primeros en identificar este sistema y relacionarlo con la inmunidad de los microorganismos.
“Francis tiene una visión global inmensa y conoce a la mayoría de los investigadores que trabajan en CRISPR Cas, por lo que ha sido maravilloso contar con su asesoramiento y con su entusiasmo cuando descubrimos estos nuevos CRISPR Cas9 del océano profundo”, admite Acinas, que celebra su amistad de años y la participación de Mojica en el artículo que están escribiendo sobre estos hallazgos.
La carrera de la investigadora se ha forjado en expediciones de grandes equipos con perfiles muy diversos: “En estos años me he dado cuenta de que la investigación, cuando pasa a una dimensión un poco más interesante, es cuando se hace de forma multidisciplinar”, concluye.